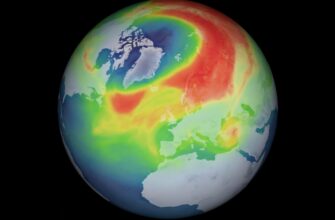
Изображения клеток сетчатки лабораторной крысы возле зрительного нерва.
Многие лекарственные вещества, потенциально эффективные для терапии глазных заболеваний, на практике не оказывают ожидаемого терапевтического эффекта. Это может быть связано как с отсутствием подходящей лекарственной формы (например, ввиду низкой растворимости веществ в воде), так и с наличием гематоретинального барьера, препятствующего проникновению различных веществ из кровотока в сетчатку. Ученые из РХТУ им. Д.И. Менделеева и институтов Германии разработали систему адресной доставки подобных лекарственных веществ и опробовали ее эффективность на крысах. Эксперименты показали, что через 15 минут после инъекции полимерных наночастиц, наполненных модельным действующим веществом кумарином-6, большая часть этого вещества проходит через барьер и распределяется по сетчатке глаза крысы. Работа опубликована в European Journal of Pharmaceutical Sciences, а ученые планируют расширить этот подход для доставки лекарств в мозг и лечения нейродегенеративных заболеваний.
С помощью технологии адресной доставки можно значительно повысить количество лекарства, которое попадает непосредственно в больной орган или ткань, что увеличивает эффективность терапии и снижает общую нагрузку на организм. Больше всего ожиданий от этого подхода связано с лечением онкологических заболеваний, но есть и многие другие болезни, где адресная доставка лекарств может быть очень полезна. Например, это различные глазные болезни – глаукома, ишемия сетчатки глаза, повреждение оптического нерва и другие. У многих веществ, потенциально эффективных для лечения этих заболеваний, очень низкая растворимость в воде и поэтому для них сложно сделать подходящую лекарственную форму. Другая проблема – гематоретинальный барьер, естественная защита организма, которая ограничивает проникновение «ненужных» молекул через стенки кровеносных сосудов в ткань сетчатки.
Возможное решение этих проблем – использование в качестве носителей лекарств небольших частиц (наночастиц), способных пройти через барьер. Молекулы лекарств при этом заключены в наночастицы, которые, попав в организм, постепенно деградируют – распадаются на нетоксичные метаболиты. С помощью такой «упаковки» можно получить наноразмерную форму лекарственного вещества, которая будет с одной стороны водосовместима, то есть позволит обойти ограничение по растворимости, а с другой стороны может адресно доставить нужное количество молекул прямо к мишени.
«Труднорастворимые вещества можно включать в наночастицы, состоящие из биодеградируемых полимеров, а потом водные дисперсии этих наночастиц использовать в качестве инъекционных лекарственных форм, удобных для внутривенного введения», – комментирует Светлана Гельперина, один из авторов работы, профессор кафедры химии и технологии биомедицинских препаратов РХТУ. – «Этот подход мы использовали в новой работе и надеялись, что наночастицы будут проникать в сетчатку. Но этого не произошло, они остались ассоциированными со стенками сосудов. При этом главное, что включенное в наночастицы модельное вещество очень эффективно проникало в сетчатку. Мы это наблюдали и фиксировали в реальном времени, – это означает, что наш подход работает и, таким образом, мы сможем доставлять и лекарственные вещества к сетчатке».
Самоотверженные наночастицы
Чтобы понять принципиальные возможности подхода ученые работали не с лекарственными веществами, а с модельным веществом кумарином-6 – красителем, который часто используют в биомедицинских экспериментах. Кумарин-6 очень ярко флуоресцирует, что позволяет легко отслеживать его концентрацию и распределение в живых тканях с помощью флуоресцентной микроскопии, фиксирующей интенсивность свечения кумарина. При этом кумарин-6 очень плохо растворим в воде, так что он может служить моделью многих малорастворимых в воде лекарственных веществ.
Для того чтобы сделать наночастицы, наполненные модельным веществом, ученые проводили многостадийное эмульгирование (смешивание) сополимеров молочной и гликолевой кислот с кумарином-6 и органическими растворителями. В результате получались однородные наноэмульсии, не расслаивающиеся с течением времени. Далее из них удаляли органические растворители и отфильтровывали, получая водную дисперсию наночастиц с включенными внутри молекулами кумарина-6.
«Такой метод получения наночастиц и мы, и многие другие исследователи применяют уже много лет. Сополимеры молочной и гликолевой кислот — это биодеградируемые фармацевтические полимеры, они производятся фармацевтическими компаниями и используются как безопасные вспомогательные вещества в различных инъекционных формах, за это их и любят исследователи», – рассказывает Светлана Гельперина. – Поскольку наше трудно растворимое в воде модельное вещество [кумарин-6] присутствует в среде в процессе формирования наночастиц, то оно, «прячась» от воды, оказывается «заключенным» в ядро частицы. При разбавлении наносуспензии, например, при введении ее в организм, это модельное вещество начинает высвобождаться из наночастиц под воздействием среды.
Ключевая характеристика таких препаратов адресной доставки – это скорость высвобождения лекарственного вещества в разных условиях или, как говорят ученые, профиль его высвобождения. Важно, чтобы высвобождение вещества проходило с нужной скоростью и наночастица, попав в кровоток, все-таки успела добраться до цели, и высвободить основную концентрацию вещества именно там.
Заглянуть в глаза
Исследователи проводили проверочные эксперименты на лабораторных крысах. После небольшой дозы анестезии животным вводили в хвостовую вену суспензию наночастиц, а потом фиксировали положение их глаза, чтобы в реальном времени отследить поведение кумарина-6 в сетчатке с помощью установки ICON (англ. In vivo Confocal Neuroimaging – прижизненная конфокальная нейровизуализация).
Проведение эксперимента по исследованию глаза крысы на установке ICON
«Это уникальная установка, которая позволяет заглянуть в глаз живой крысе, увидеть и измерить распределение модельного вещества в сетчатке и соседних сосудах», – отмечает Светлана Гельперина. – Установка представляет собой микроскоп, оснащенный источником возбуждения и регистрации флуоресценции, и специальные фокусирующие механизмы. Крыса во время измерений обездвижена, в глаз периодически капают капли, чтобы он не пересыхал, а мы наблюдаем за тем, как частицы циркулируют в крови и что с ними происходит потом».
В результате ученые установили, что наночастицы остаются внутри сосудов и не проходят через барьер. Но кумарин-6, который они выделяют в сосудах, питающих сетчатку, проходит через стенки сосудов в сетчатку глаза и дальше там распространяется. По данным измерений, уже спустя 15 минут после инъекции почти весь кумарин переходит из сосудов и распределяется по сетчатке, что позволяет предположить высокую скорость действия таких препаратов при использовании не модельных, а реальных терапевтических средств в будущем.
Распределение концентрации кумарина-6 в глазу крысы в реальном времени: спустя 90 минут после инъекции вещество полностью находится в сетчатке, а не в сосудах (BV)
Предложенный способ адресной доставки лекарств достаточно прост и, по словам ученых, может быть быстро и эффективно масштабирован до создания производственной линии. В дальнейшем исследователи планируют не только продолжать работы с лекарствами для терапии глазных болезней, но и развивать этот подход уже для заболеваний центральной нервной системы, в частности для лечения глиом – опухолей мозга.
Источник: New-Science.ru